
香港文匯報訊(記者 楊梓穎)香港科技大學(科大)研究團隊在生物學 RNA 沉默機制研究中取得突破性發現,發現人類體內關鍵核酸酶DICER能精準調控微小核糖核酸(microRNAs, miRNA)的機理。這一科研突破將有助推動基因調控研究的發展,為深入了解癌症、免疫系統疾病及遺傳疾病機制提供全新角度。這項研究由科大生命科學部副教授阮俊英領導,並由博士生Minh Khoa NGO與Cong Truc LE共同完成,研究成果已刊登於國際頂尖學術期刊《Nature》。
RNA(核醣核酸)在細胞內負責傳遞和執行DNA遺傳訊息,並參與蛋白質製造及基因表現調控,甚至在某些病毒中充當遺傳物質。DICER則是RNA沉默系統中的核心核酸酶,猶如一把「精密剪刀」,可將雙股RNA切割成極短片段,讓細胞識別並關閉錯誤或多餘的基因訊息,猶如在文章中標記與刪除錯字。
科學界一直關注DICER如何做到高精準度切割。科大團隊運用高通量生化實驗及冷凍電子顯微鏡技術,在原子解析度下揭示DICER與RNA的相互作用,發現DICER在切割前會先進行構形調整,把RNA引導至正確位置,再透過酵素內部的5′端結合口袋的胺基酸精準定位,最後進入「切割就緒」狀態。
Minh Khoa Ngo表示:「冷凍電子顯微鏡技術讓我們在原子解析度上觀察RNA底物與DICER的結合過程,這些分子影像清晰展現了該核酸酶針對不同RNA序列做出的動態調整,從根本上改變了我們對其功能的認知。」
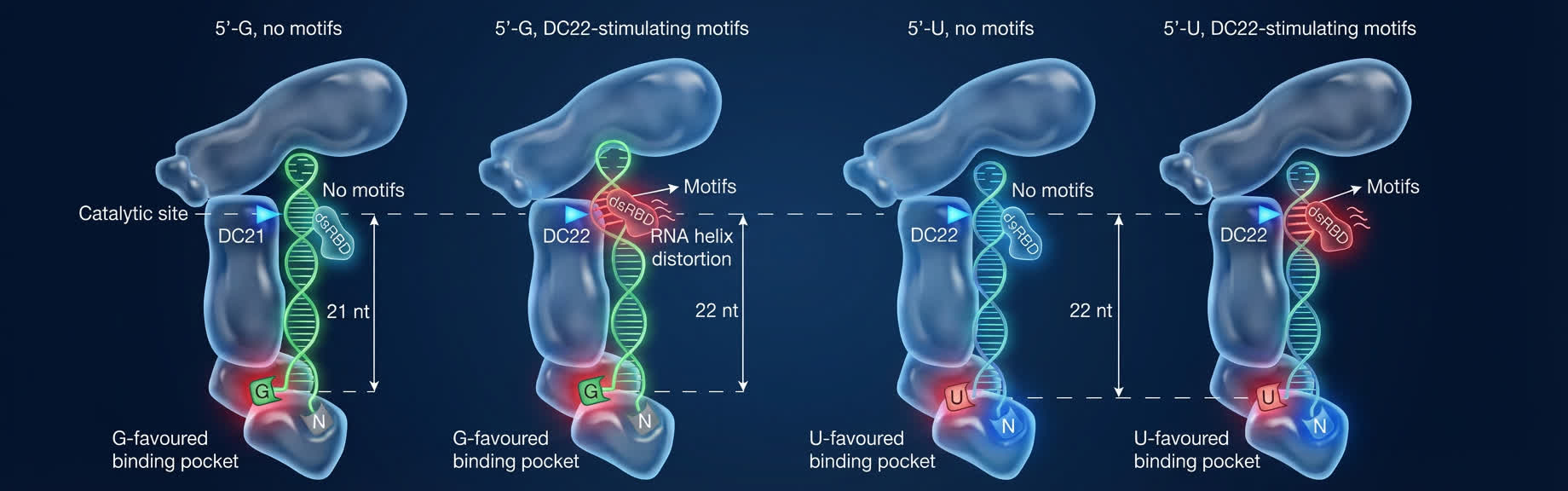
研究更首次發現,除已知偏好辨識尿嘧啶(U‑favoured)的5′端結合口袋外,DICER還具有一個全新的、偏好辨識鳥嘌呤(G‑favoured)的5′端結合口袋。兩者共同構成「雙口袋機制」,決定DICER在不同位置進行切割,為闡釋DICER如何適配並切割不同RNA序列提供了全新的理論依據。
阮俊英表示,這項發現的影響遠遠超越生物學基礎知識,不僅揭示了DICER如何整合5′端核苷酸種類、RNA結構基序(motifs),以及酵素內部結構域的動態變化以維持切割精準度,也為改良 RNA 疾病治療藥物及基因沉默技術奠定基礎,進一步為解析DICER相關遺傳疾病成因提供了新的研究方向。





 贵公网安备52011302005168号
贵公网安备52011302005168号