2025年,中国在药品审批与研发输出方面实现历史性跨越,首次在年度创新药批准数量上超越美国。国产CDK4/6抑制剂密集上市、流感新药迎来国产元年等趋势,彰显中国在热门靶点与细分适应症上的快速突破。同时,中美新药上市时间差显著缩短,部分跨国药企产品实现全球同步开发甚至“中国首发”,进一步凸显我国在全球研发与供应链中的地位提升。此外,美国上市新药延续高创新特质,在小分子精准调控、核酸疗法、ADC等前沿领域持续引领技术方向。本文将从治疗领域、创新质量、上市时差等维度,对中美2025年获批新药作简要分析。
主要治疗领域相近
从治疗领域分布看,抗肿瘤、免疫系统疾病、抗感染、内分泌与代谢疾病是中美获批新药最集中的四大领域。抗肿瘤仍是最热门的治疗领域,尤其在中国,比重显著高于其他治疗领域。
从适应症看,中国抗肿瘤新药主要集中在乳腺癌与非小细胞肺癌。其中,乳腺癌创新药大量上市主要得益于CDK4/6抑制剂的密集获批。例如,轩竹生物的吡洛西利、奥鸿药业的伏维西利、嘉和生物的来罗西利在一个月内相继获批。这显示了本土企业在热门靶点上的快速跟进能力,但也暗藏激烈竞争的风险。截至2026年2月4日,国内获批上市的CDK4/6抑制剂已达10个。值得一提的是,正大天晴的库莫西利是全球首款CDK2/4/6抑制剂,作为新一代CDK抑制剂,该药有望破解传统CDK4/6抑制剂在耐药、骨髓抑制等方面的临床痛点。
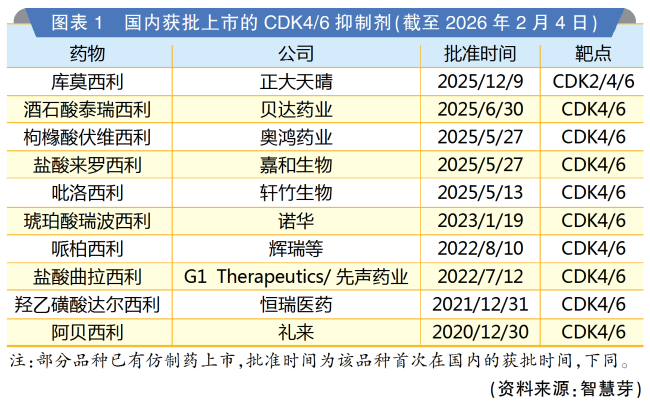
免疫系统疾病也是新药研发布局的火热领域,尤其在美国,是仅次于抗肿瘤的第二大治疗领域,且多数为罕见病药物。中国获批新药中,免疫系统疾病药物数量位列第四,其中不乏实现国产突破的新药。
值得关注的是,2025年成为BTK抑制剂在自免领域的破局之年。赛诺菲的Wayrilz(rilzabrutinib)率先在美国获批免疫性血小板减少症(ITP)适应症,诺华的Rhapsido(瑞米布替尼)紧随其后拿下慢性自发性荨麻疹(CSU)适应症。
自免疾病作为仅次于肿瘤的全球第二大市场,一直是药企的必争之地。BTK抑制剂在自免领域的巨大潜力吸引了众多药企布局,其中不乏艾伯维、赛诺菲、诺华、礼来、阿斯利康、罗氏等制药巨头。在这场全球竞速中,国产力量也在跟进,已布局的企业包括百济神州、诺诚健华、正大天晴、恒瑞医药等。从研究进度来看,诺诚健华、百济神州、邦顺制药的产品处于第一梯队,均已进入Ⅲ期阶段。
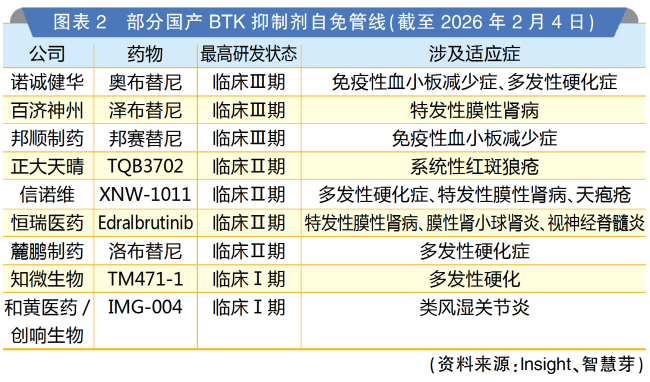
抗感染也是中美获批新药的重要板块,但适应症存在差异。其中,美国获批的抗感染新药主要为疫苗与抗菌药,中国获批的新药主要为治疗流感及丙肝的抗病毒药。
2025年也被称为“国产流感新药元年”,多款国产RNA聚合酶抑制剂密集获批,包括科睿药业的玛舒拉沙韦、众生睿创的昂拉地韦、征祥医药的玛硒洛沙韦以及健康元的玛帕西沙韦。其中,昂拉地韦是全球首款PB2靶点抑制剂,其余3款药物均为与玛巴洛沙韦相同的PA靶点抑制剂。这些新药不仅有助于提升我国应对本土公共卫生需求的能力,也将为以奥司他韦与玛巴洛沙韦为主导的流感抗病毒药物市场格局带来新变化。
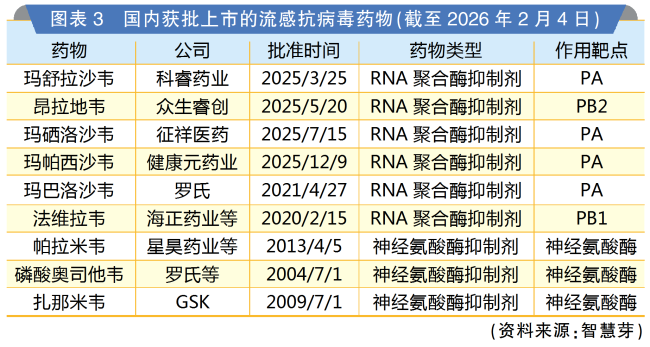
美国新药FIC占比四成
从创新含金量看,2025年中美批准的新药中,不少在相关领域实现了里程碑式突破。多个长期缺乏进展的疾病领域迎来关键药物,新兴技术平台也逐步走向成熟。尤其美国作为全球创新药的主要市场,虽然CDER批准的新药数量略有减少,但首创新药(first-in-class,FIC)占比达到四成。一方面,ADC、双抗、核酸药物等前沿技术持续发力;另一方面,非阿片类镇痛、非囊性纤维化支气管扩张症治疗、非激素更年期治疗等方向的突破,填补了存在已久的临床需求缺口。
在中国,FIC产品也是注册审批的工作重点。2026年,国家药监局将对新机制、新靶点创新药在沟通交流、临床试验、注册申报、审评审批全链条强化服务支持,助力创新药中国首发。
2025年中国批准的新药中有11个FIC产品,其中4个为我国自主研发。与美国相比,虽然我国对FIC创新药全球首发的吸引力,以及本土企业在前沿创新方面的能力有待进一步加强,但近年来中国上市创新药的质量已经得到显著提升。这不仅体现在创新药数量和技术类型的多样性,也有更多突破性疗法、源头创新药物上市,且越来越多的中国上市新药在全球保持了研发进度的领先性。
例如,2025年获批新药中,信达生物的玛仕度肽是全球首个GCG/GLP-1双受体激动剂,IL-12/IL-23双靶向单抗、IL-1β单抗、Bcl-2抑制剂等领域均迎来了首个国产新药。
上市时差“同频”渐显
从新药上市的时间差看,跨国药企的创新成果在中国加速落地。2025年,有7个新药在中美两地均实现上市准入,获批时间间隔最短的药物仅相差3天。
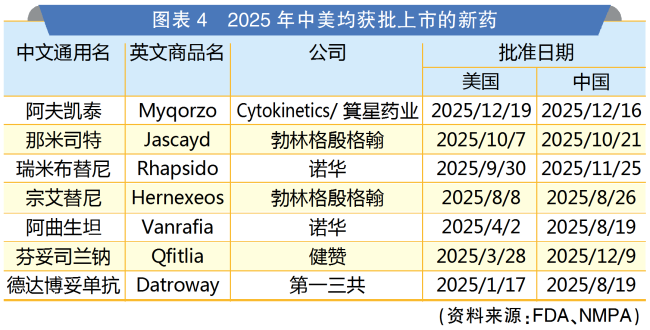
新药中美上市“同频”趋势渐显,一方面,跨国药企受益于本土化研发布局深化及中国审评审批制度改革,其新药上市申请能在中国同步提交,甚至中国首发。例如勃林格殷格翰,其抗肿瘤新药宗艾替尼(Hernexeos)与特发性肺纤维化新药那米司特(Jascayd)分别于2025年8月与10月在美国及中国获批,中美获批时间间隔不到三周。
另一方面,国内企业进一步融入全球创新链,通过国际研发合作,加速将海外创新药引进国内。例如梗阻性肥厚型心肌病治疗药物阿夫凯泰(Myqorzo)在中国实现了全球首发,早于美国和欧盟等主要医药市场。该药最初由美国Cytokinetics公司研发,2020年7月箕星药业获得其大中华区权益,2024年12月赛诺菲通过与箕星药业合作,取得该药在大中华区的独家开发与商业化权利。阿夫凯泰的国内首批上市,既是中国药品审评体系效能提升的缩影,也是全球新药研发与商业合作网络日益紧密的体现。
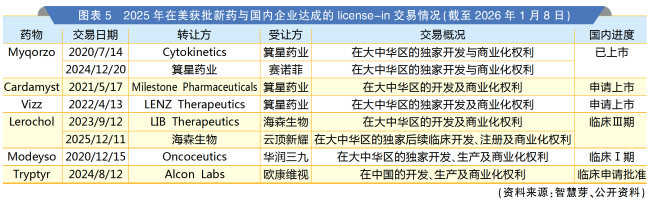
据不完全统计,除了阿夫凯泰,还有5个2025年在美获批上市的新药已达成与国内药企的license-in交易。其中,箕星药业分别于2021年、2022年引进的阵发性室上性心动过速治疗药物Cardamyst与老花眼治疗药物Vizz进展最快,均已在国内提交了上市申请。此外,从LIB Therapeutics引进的第三代PCSK9抑制剂Lerochol已进入Ⅲ期临床阶段,华润三九引进的抗肿瘤新药Modeyso与欧康维视引进的干眼症新药Tryptyr尚处于早期阶段。
结语
2025年是全球医药创新格局加速演进的一年。从数据上看,中国创新药获批数量首次实现对美国的超越,国产创新药对外授权总额也创下新高,标志着中国已从全球医药创新的重要参与者,成长为不可忽视的驱动力量。这一成绩的取得,是持续深化的审评审批制度改革、日益成熟的产业生态与资本市场,以及企业研发实力系统性提升共同作用的结果。
同时,本土首创新药占比偏低、热门靶点扎堆研发、临床前原始创新能力不足等问题,仍是制约我国从“制药大国”迈向“制药强国”的关键瓶颈。未来,如何从“fast-follow”向“first-in-class”跨越,如何在靶点发现、机制研究等源头创新环节实现突破,如何平衡创新药的临床价值与商业价值,将成为中国医药产业需要攻克的核心课题。




 贵公网安备52011302005168号
贵公网安备52011302005168号